研 究
| 癌、移植、再生の3分野を中心としています。 また長崎大学全体を一つのラボと考え、他講座と広く有機的に連携し、研究を続けています。 毎週金曜日に教授を中心とした実験カンファランスを行っており、活発な議論を行いながら、各自の細かい方針を決定しています。 |
 |
|---|---|
| カンファランスの風景 |
腫瘍外科の研究
腫瘍外科では教室独自の研究に加え、医学部・原研基礎講座、薬学部、歯学部、工学部、などと連携し、講座の枠を超えた様々な分野との双方向性の共同研究を、自由闊達に往来しながら行い、常にあらゆる分野との研究にも迅速に対応できることを目指している。さらには、国内外の研究施設との共同研究も積極的にすすめており、具体的には九州大学、佐賀大学、自治医科大学先端医療技術開発センター、東京理科大学薬学部、米国のCincinnati Children's Hospital Medical Center、Yale University Bioengineering Laboratory Center、Cedars-Sinai Pulmonary Stem Cell Research Laboratory Centerとは頻繁に情報交換を行いつつ、共同研究の成果を達成している。
大学院生や研究生は、週に1回のカンファランスを行いながら、研究の進展と現在の問題点、これからの方向性を協議し、月1回の研究抄読会を行って、広く深い知識を身に着けることを可能としている。
大学院生や研究生は、週に1回のカンファランスを行いながら、研究の進展と現在の問題点、これからの方向性を協議し、月1回の研究抄読会を行って、広く深い知識を身に着けることを可能としている。
当科の研究内容の紹介
| 再生および生体医工学に関する研究 |
|---|
| 当科は、肺および気管、気管支の再生研究を続けてきた。また、創傷治癒やバイオ被覆材、手術による肋間神経障害の科学的測定等、様々な方面で研究を続けている。 【液性因子(KGF)による気管軟骨、肺の再生】 これまで我々は、肺の成長因子の1つであるKeratinocyte growth factor(KGF)を用いて肺上皮の再生の研究を進めてきた。KGFは肺上皮細胞に特異的に作用し、HGFの20倍、βFGFの13倍の作用があるとされ、さらに間葉系への作用はほとんどみられていない。KGF蛋白による肺胞上皮、肺胞の再生可能であることを確認し、さらに量産が可能なKGF遺伝子を導入したプラスミドを繰り返し遺伝子導入することで、ラットにおける肺の再生を確認した。 呼吸器外科領域における合併症の中でも、気管支胸膜瘻は時に致死的となりうる。これまでの実験結果より、肺の成長因子であるKGFが気管、気管支の創傷治癒において重要な鍵を握る軟骨細胞と上皮細胞の両者の再生・修復因子であることが解明されてきた。現在、気管吻合モデルと気管培養モデルを作成し、除法性シートに含有させたrecombinant KGFを局所投与することにより創傷治癒過程における気管及び気管支軟骨と気道上皮細胞への再生促進効果を検討している。 【脱細胞化及び再細胞化による異種肺からのヒト肺の創出】 肺そのものを作成することは現在の科学技術では不可能であるが、"細胞を入れ替える"技術を使って、豚等の異種の肺からヒトの肺を創出できるかもしれない。我々はラットの肺を脱細胞化(Decellularization)し、ヒトなどの他の動物種の肺細胞で再細胞化(Recellularization)する技術をYale大学より導入し、現在研究中である(下のシェーマ参照)。今後は、他の医療機関と共同研究を進めながら実験モデルを大型動物の気管や肺に移行し、使用細胞としてさまざまな幹細胞やiPS細胞を使って、同技術を確立していくことを目標にしている。 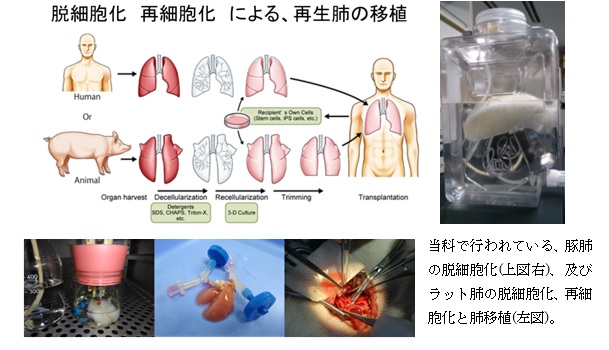 【Bio-3Dプリンターを用いた人工臓器、気管、食道の作製】 再生医療が進歩をみせるなかで、細胞レベルでの再生医療は臨床試験への試みもはじめられているが、最終的な目標である人工臓器作製はまだ遠い目標である。特に人工物や免疫抑制剤を用いない、自己細胞からの臓器作製は、理想的な人工臓器であり、最終目標でもある。我々の共同研究者は、この問題を解決するため、Bio3Dプリンターを開発した。細胞の塊(スフェロイド)を作成後、個のプリンターにて立体臓器を構築し、培養することで、自己細胞からの臓器作製が可能となった。現在血管の構築が可能となっている。これをさらに進歩させ、我々の分野である肺、気管支、食道の自己細胞による人工臓器作製を試みている。  【生体医工学】 我々は以前より京都大学再生医科学研究所と共同して、生体分解性高分子化合物の臨床への応用を研究してきた。現在、動物実験において有用性が確認された案件は、①肺胞瘻防止 ②胸腔内術後癒着防止 ③腹腔内術後癒着防止の3件である。今後も膵液瘻や胆汁瘻の防止への応用を検討していく予定である。 また我々は、医工連携、産学連携分野にも進出し、リンパ節転移診断キットや鏡視下手術関連デバイスの開発を進めている。現在まで特許2件申請中、実用新案を1件取得しており、今後もさらに新規医療機器の開発を行っていく予定である。 科学研究補助金採択課題
過去5年間の主な研究論文(欧文150編中)
|
| 移植に関する研究 |
|---|
| 当科は、日本で2番目に肺移植を行った施設でもあり、1990年代より、精力的に肺移植研究を続けてきた。当時は異種移植や大型実験動物による肺保存液の研究が中心であったが、研究の幅を広げ、免疫抑制剤の気管内投与、T細胞抑制因子の肺移植拒絶抑制に対する効果等の研究を続けてきた。現在は、薬剤による肺虚血再還流障害の抑制や、幹細胞の移植肺への影響の研究を行っている。 また、当科は2005年より肺移植の認定施設となっており、臨床応用に向けて、上記の研究を精力的に進めている。 “Polymerase Inhibitor (PJ34) Reduces Pulmonary Ischemia-Reperfusion Injury in Rats” (Hatachi et al. Transplantation 2014) 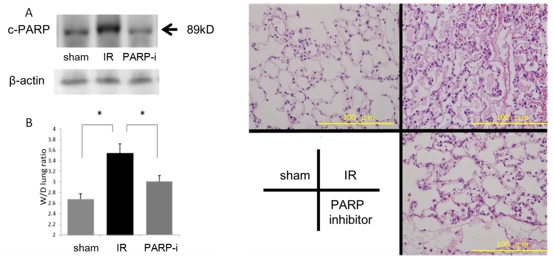 ラット左肺の虚血再灌流(IR)モデルにおいて、PARP阻害剤使用群(PARP-i群)では、肺の活性型PARP蛋白は減少し、肺の重量増加は軽減した(左上図)。病理像では、IR群に比べ、PARP-i群で肺の虚血再灌流障害は抑制された(右上図)。 科学研究補助金採択課題
過去の主な研究論文(2007年より)
|
| 癌および腫瘍に関する研究 |
|---|
| 対象:肺癌、消化器癌、内分泌癌 肺癌では、肺癌分子標的治療のターゲットであるEpidermal growth factor receptor遺伝子変異と5-FU代謝関連酵素への関係について、精力的な研究を行っており、将来のオーダーメード治療を目指している。人類遺伝学講座とは、転移性肺癌と多発肺癌の鑑別診断を遺伝子プロファイルの違いによって判定する研究手法を確立し、家族性の肺癌家系からは新しいdriver mutation遺伝子異常を探索している。臨床研究では、経口抗癌剤であるS-1に着目し、県内関連施設との多施設共同研究として肺癌術前・術後補助療法の第Ⅱ相臨床試験を行っている。また、海外との共同研究も行っており、Cincinnati Children’s Hospital Medical Centerの基礎的研究と当科の肺癌切除患者の臨床データによって、患者の予後の予測や治療に直結する新しい研究分野を開拓している。 消化器癌では、食道癌、胃癌において抗癌剤耐性遺伝子と治療効果との関連や新規バイオマーカー探索に関して研究している。肝胆膵領域における新規バイオマーカーの探索、外科治療後の予後予測マーカーとしての分子生物学的マーカーの研究を行い、特に癌の新生血管因子と発現が有力な予測因子であるとの報告を行ってきた。Flow cytometry、FISH法、CGH法を用いた癌の染色体異常、抗がん剤耐性遺伝子、p53遺伝子異常については過去30年間の多大な成果を報告している。現在、文科省研究費における癌の早期診断のための尿中ペプチド断片の網羅的解析を、大阪大学・宮崎大学・国立がんセンター東病院との多施設共同研究に参画している。難治性の胆道癌における局所制御を向上させるために、2001年より光線力学的療法(PDT)の臨床試験を開始し、2009年より第二世代のPDT臨床試験へとつなげ、その有用性について基礎的・臨床的成果を欧文8編、邦文12編で報告している。現在、さらに治療効果を高めるための第三世代の光増感剤を用いたPDT研究に着手している。特殊な胆管癌の特性を解明するために、国内では日本胆道学会研究班および金沢大学形態機能病理学と、国外ではYale大学肝臓研究部門ならびにLeuven大学病理との共同研究を実施している。大腸癌では潜在的な癌微少転移診断としての1-CTPマーカー研究、血液中のp53発現の解析を行っている。動注化学療法の肝内転移制御については高い有効性を示し、この分野の権威である米国Memorial Sloan Kettering 癌センターからレビュー論文での高い評価を得ている。 内分泌分野では、甲状腺癌の微小浸潤癌機構のゲノム解析を行っている。乳癌では、腋下センチネルリンパ節への潜在的な転移を、リンパ節切片の洗浄液から極めて簡便・迅速に診断するSemi-dry dot blot法を開発し、高い精度での転移診断の成果を得たことで、臨床での実用化に向けた検査キット化に着手している。 科学研究補助金採択課題
過去5年間の主な研究論文(欧文150編中)
|
| 小児外科関連の研究 |
|---|
| 【胆道閉鎖症早期発見としての新生児尿中硫酸抱合型胆汁酸(USBA;Urinary Sulfated Bile Acid)の測定】 肝細胞内でコレステロールより合成された胆汁酸は肝内胆管から肝外胆管を経由して十二指腸内に排泄されるが、胆道閉鎖症などの肝外胆管が閉塞する疾患では、肝細胞内に鬱滞した胆汁酸が硫酸抱合を受けて血液中に溶出し糸球体で濾過されて尿中に排泄されることになる。胆道閉鎖症は出生直後から肝外胆管が閉塞する原因不明の疾患で、国内で年間100人前後が発症しおり、生後60日までの葛西手術(肝門部空腸吻合)が予後を左右するため、早期発見と早期手術が提唱されている。診断は遷延性黄疸や灰白色便などの臨床所見が中心で客観的指標が存在しないのが現状である。 長崎大学腫瘍外科・小児外科グループでは2006年から長崎県産婦人科医会の協力の下に新生児の採尿検査によるUSBA測定を行い、胆道閉鎖症の早期発見の取り組みを開始した。 2014年6月現在県内の産婦人科病院・医院30施設のUSBA測定参加により、県内出生数の約60%の新生児・乳児をカバーしている。USBA測定開始後、5例が胆道閉鎖症と診断され内4例にUSBA測定が関与していた。USBA測定により胆道閉鎖症の早期発見数増加が期待されるが、また胆道閉鎖症の早期の病態解明への応用も期待される。 【カテーテル関連血流感染症に対する研究】 ①エタノールロック療法 1.カテーテル内のバイオフィルム研究 中心静脈栄養や抗がん剤などの化学療法が長期間必要な場合、中心静脈ポートなどの長期留置型カテーテルが留置される。中心静脈カテーテルの重篤な合併症の一つにカテーテル関連血流感染症(=カテーテル敗血症)が挙げられ、カテーテル内に形成されたバイオフィルムが原因と言われている。これまでの標準治療は、抗生剤投与とカテーテル抜去であったが、カテーテル再挿入などの負担を軽減する目的で、カテーテル温存療法が試みられるようになってきている。エタノールロック療法はその1つで、70%に希釈をしたエタノール溶液をカテーテル内に4~24時間充填し、連続5日間繰り返し行う治療法である。まだ標準治療ではないが、その有用性は邦文3編で報告しており、今後は多施設共同研究を視野にいれた臨床研究である。 また、上述のようにカテーテル関連血流感染症の原因は、カテーテル内に侵入した細菌が形成したバイオフィルムであり、カテーテル内のバイオフィルムおよびエタノールの役割に関する実態は明確になっていないのが現状である。その実態を、基礎的・臨床的に調査および評価に着手している。 |


