脳梗塞後に働いているシグナル伝達分子の役割を解明
・スフィンゴシン 1-リン酸(S1P)は脳梗塞後の血液脳関門機能障害に関与する
・脂質異常症治療薬プロブコールには血液脳関門保護作用がある
Nakagawa et al., Mol Neurobiol. (2019)
日本では今後ますます高齢化が進み、脳卒中、認知症、癌など加齢に関連した疾患が増加することが予測されます。なかでも脳卒中は死亡原因の第4位を占めているだけでなく、寝たきりの最大の原因となっており、その治療薬開発は重要な課題となっています。脳梗塞では脳の血管が閉塞し、グルコースなどの栄養や酸素を十分に脳内に届けることができずに神経細胞が障害を受けます。また、脳の血管自体にも障害が起こり、通常は脳内に漏れ出ないような血液内の成分が脳内に移行し、障害を悪化させてしまいます。我々は、脳の血管を保護することは、脳内の環境を維持し、神経細胞の保護や脳梗塞の治療につながると考えて研究を行ってきました。
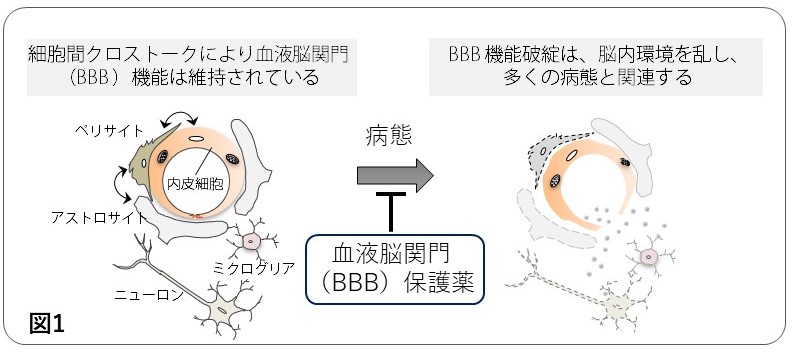
脳の毛細血管には、血液脳関門(Blood-Brain Barrier, BBB)と呼ばれる特性が備わっており、血管内の循環物質の脳内への移行を調節することで、脳内環境を維持する役割を持っています。BBBは脳毛細血管内皮細胞と周皮細胞(ペリサイト)、アストロサイトの3種類の細胞で構築されており、これらの細胞間の情報のやりとり(クロストーク)により維持されています(図1)。このクロストークはBBBの機能を維持するために重要であることが知られていますが、脳梗塞後にどのような役割を持つのかについては不明な点が残されていました。
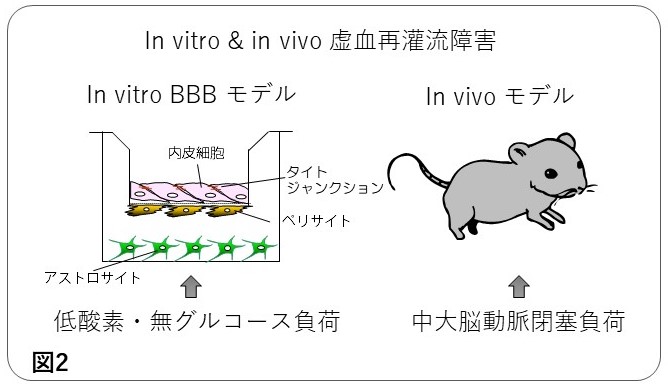
これまでの研究から、培養細胞でBBBを再現した実験系(in vitro BBBモデル)を一時的に低酸素、無グルコースの状態(ストレス状態)におく(図2)とBBBの機能が低下することが知られています。この状態は脳梗塞の状態に似ており、「in vitro虚血再潅流障害」と呼ばれています。我々が実験したところ、脳毛細血管内皮細胞単独のin vitro BBBモデルよりも、3種類の細胞が存在するin vitro BBBモデルにおいて、「in vitro虚血再潅流障害」が悪化することを見出しており、ペリサイトやアストロサイトから放出される細胞間のシグナル伝達分子(クロストーク因子)が、脳梗塞後のBBB機能低下と関係するのではないかと考えました。
今回、私たちは脳梗塞でのクロストーク因子として、スフィンゴシン 1-リン酸(sphingosine 1-phosphate, S1P)に注目して研究を行いました。S1Pは生体内に存在する生理活性を持った脂質分子の一つで、免疫系や血管系で重要な働きをしています。また、心臓などでは心筋梗塞の時に多く産生されることも報告されています。S1Pの脳卒中での役割を検討するために、(1)in vitro BBBモデルを用いた「in vitro 虚血再灌流障害」と(2)麻酔したマウスの脳の血管を一時的に閉塞して(中大脳動脈閉塞)、その後の脳の状態を調べる「in vivo 虚血再灌流障害」を用いました(図2)。「in vitro」 とは試験管や培養皿の中で行う実験系、「in vivo」とは生体に近い状態で行う実験系をさすラテン語由来の言葉です。
In vitro BBBモデルを用いた検討により、「in vitro虚血再灌流障害」はS1Pを合成する酵素(スフィンゴシンキナーゼ)やS1Pの輸送に関わるタンパク質(ABCA1輸送体)を増加させ、内皮細胞、ペリサイトおよびアストロサイトからの細胞外へのS1P放出量を増加させることがわかりました。また、S1PはBBBのバリアー機能を低下させることが明らかとなりました。更に、S1P合成酵素(Sphk1)を阻害する薬(SKI-II)やABCA1輸送体を阻害する薬(プロブコール、Probucol)により、BBBの「in vitro虚血再灌流障害」が軽減することも確認しました。以上のことから、脳の毛細血管を構成する細胞は「in vitro虚血再灌流障害」の際にS1Pの産生を亢進させ、BBB機能を低下させること、SKI-IIやプロブコールはBBBの機能障害を改善する働きがあることが示唆されました(図3)。
次に、BBBを保護する効果のあったプロブコールの作用を、マウスを用いた「in vivo 虚血再灌流障害」の実験で検討しました。その結果、実験的に脳梗塞を起こしたマウスでは、正常なBBBでは通さない分子が血管の内から外へ漏れ出るようになりますが、プロブコールを脳梗塞の直後に投与するとBBBの機能が正常に保たれ、脳梗塞を起こした脳の領域が減少することが観察されました。更に、BBBの透過性を調節する分子として、タイトジャンクションと呼ばれる、細胞と細胞を密着させる構造が重要であると考えられています。このタイトジャンクションを構成するタンパク質は脳梗塞により低下するものの、プロブコール投与により、低下が抑えられることも明らかになりました。このようにプロブコールは「in vitro」だけでなく「in vivo」でも虚血再灌流によるBBBの機能障害を改善する働きがあることが確認できました。
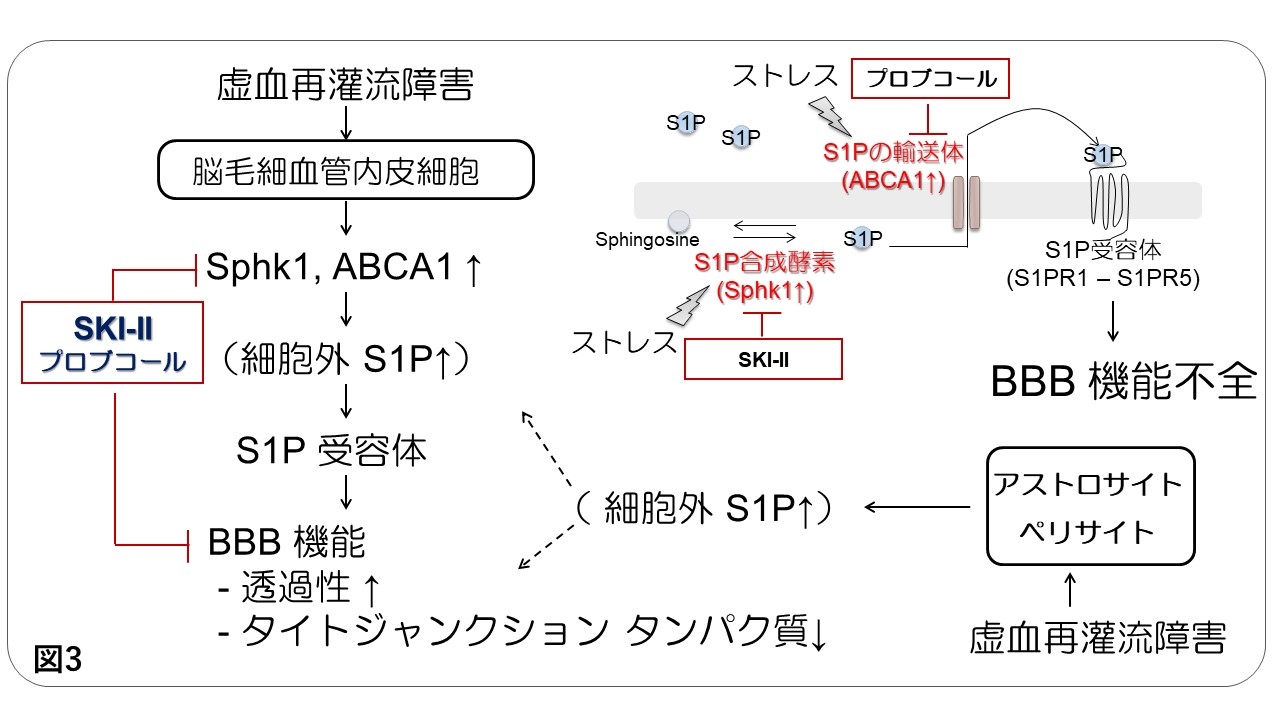
これらの結果から、S1Pは脳梗塞後に増加して、BBB機能を低下させるシグナル伝達分子として働くことが考えられました(図3)。また、「プロブコールにはBBBの保護薬としての可能性があること」も示されました。プロブコールはこれまでに脂質異常症治療薬として使用されており、脂質低下作用や抗酸化作用が注目されています。この研究により、プロブコールにはこれらの作用に加え、BBBを保護する作用があることが示唆されました。研究成果が医療に応用されることを期待します。


